最近血糖値が下がらない。グルカゴンが高血糖の原因であることは知っている。
糖尿病患者の殆どが、グルカゴンの分泌値が高いことも知っている。
わたしは器質的に食後高血糖を起こすので、それを避けることに気をつけている。
以下、出典: フリー百科事典『ウィキペディア(Wikipedia)』を抜萃。
グルカゴン (Glucagon) とは、29のアミノ酸残基からなるペプチドホルモンの一種であり、タンパク質およびアミノ酸(Amino Acid)の代謝に重要な機能を持つ。分子量3,485。インスリン(Insulin)とともに血糖値(Blood Glucose Levels)の制御に関係する重要なホルモンの一つである。
インスリンは血糖値を低下させるが、グルカゴンはそれとは逆に血糖値を上昇させるホルモンの一つであり、人体が低血糖になるのを防ぐため、肝細胞に働きかけることでグリコーゲンを分解するよう信号を送り、血糖値の上昇を促進する(血糖値を低下させるホルモンはインスリンのみであるが、血糖値を上昇させるホルモンはグルカゴン以外にも複数備わっている)。主に膵臓のランゲルハンス島のA細胞(α細胞)で生合成・分泌されるほかに、消化管からも分泌される。
絶食中か、低血糖になるか、タンパク質を摂取することでも分泌が誘発される。逆に、炭水化物および砂糖を摂取して高血糖になると、分泌は抑制される。高タンパク食、高脂肪食を摂ると、血漿グルカゴンの上昇がみられる。しかし、単純脂肪経口投与では、グルカゴン分泌の増加は起こらない。
別のホルモンであるソマトスタチン、セクレチンはグルカゴンの分泌を抑制するが、その際には成長ホルモン、チロキシン、糖質コルチコイド、コレシストキニン、ガストリンの分泌が刺激される。
神経性因子として、迷走神経はムスカリン様作用により、グルカゴンの分泌を促進する。交感神経はβ作用によるグルカゴンの分泌の促進と、α作用によるグルカゴンの分泌を抑制する両方の作用を持つが、通常は分泌促進作用が優勢となる。
異論あり。
“炭水化物および砂糖を摂取して高血糖になると、分泌は抑制される。“
これは、高血糖になるとインスリンの分泌が促進され、グルカゴンの分泌が抑制されるという従来の考え方だ。しかし、この考え方はすでに古びた辞書のように朽ちている。高血糖になっても、グルカゴンの分泌は抑制されず、さらに高血糖を生む症例が確認されている。インスリンとグルカゴンは必ずしも拮抗ホルモンではないのだ。
β細胞のインスリン分泌を止め、さらにα細胞のグルカゴン分泌を止めると、どうなるか。マウスの実験では、血糖値は上がらない。つまり、1型糖尿病の人でも、グルカゴンの更新を抑制すれば、血糖値が異常に上がることはないということだ。血糖値が異常に上がる原因は、インスリン不足のせいではなく、グルカゴンの亢進にあるというわけだ。
最近の私の血糖値の推移を見ればわかる。正確な数字は出さないが、例えば、朝の血糖値が200だったとする。軽く食事を摂ると230になり、3時間を過ぎても下がらない。やがて次の食事を摂ると、200に下がる。散歩をしてくると、180になったりもするが、下手な筋トレをすると、220に上がる。中性脂肪は増えているのでインスリンは出ている。しかし、血糖値は有意に下がらない。グルカゴンも亢進しているということではないのか。これを医学では、インスリン抵抗性と呼んでいるのではないか。このことについては全くの妄想だが。
これはどういうことだろう。
考えに考えた。
私は軽い糖質制限を続けている。そして、最近は肉も食べることが少なくなった。そして、そう、カロリーが足りていないことに気づいた。糖質を削減した分のカロリーが蛋白質や脂質で補えていないのだと思う。だから、グルカゴンは栄養不足の私の血糖値を糖新生も使って上げているのではないか。わたしは胃を切除しているので、食事直後に血糖値スパイクを起こしやすい。だから、糖質を制限している。(過剰なインスリン分泌は活性酸素を生じ、細胞を傷つけてしまう。)それが、いつしか、カロリー不足に繋がり、グルカゴンが亢進したのだろうか。
次に思い当たるのは、昨年末からの交感神経緊張状態。ストレスの継続だ。そんなに大きく食事が変わったわけではないが、交感神経が緊張を続けているのでグルカゴンが亢進しているのではないか。
そして、心臓血管手術後の不整脈を抑えるために、わたしが服薬しているβブロッカーの作用。βブロッカーはグルカゴンを更新させる場合がある。医師によっては、低血糖の予防としてβブロッカーを使う医師もいる。
何が根本的な原因かは、わたしにはわからない。残念ながらわからない。
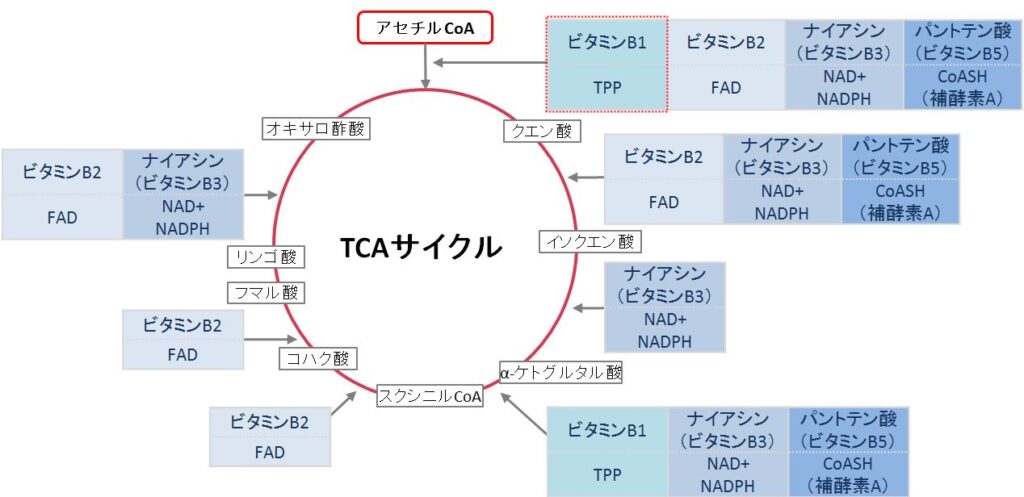
糖質制限をされている方は注意してほしい。糖質制限で削減したカロリーは、他の食物で補わなくてはいけない。「糖新生があるから大丈夫」という医師もいるが、糖新生などを使っては駄目なのだ。筋肉が痩せ、基礎代謝が下がってしまう。脂質とタンパク質を摂り、ケトン体質になる、これが糖質制限の目的であったはずだ。脂質は代謝の際にアセチルCoAになり、ミトコンドリアのエネルギーになるが、糖質は解糖系を使い、その後にアセチルCoAになる。順調にアセチルCoAにならなかった糖質は乳酸として残り、細胞を酸化に導いてしまう。
“糖新生とは、ヒトや動物が、グルカゴンの分泌をシグナルとして、ピルビン酸、乳酸、糖原性アミノ酸、プロピオン酸、グリセロールなどの糖質以外の物質から、グルコースを生産する手段・経路である。”
出典: フリー百科事典『ウィキペディア(Wikipedia)』
今日の記事は、あくまでも私の最近の体調不良の原因を考えたわたしの頭の中を描いたものに過ぎない。糖質制限をする方は、それぞれの身体や環境を考えた上で、自己責任で行って欲しい。
それにしても人体は難しい。今の細分化した医学では人体の解明などできないだろう。医師はわたし達の血液検査を正常にするために薬を処方することしかできない。血糖値の高値が過剰なインスリンを分泌させ、細胞を傷つけてしまう。しかし、血糖値は検査しても、インスリンの値を検査する医師に、わたしは会ったことがない。
ただ、身体は間違わない。間違うのは、わたし達の生活や思考なのだと思われる。身體の発する症状から身體の声を聞き取るしかできないのだ。
群馬大学 生体調節研究所・代謝シグナル解析分野 教授 北村 忠弘
https://www.niigatashi-ishikai.or.jp/newsletter/academic/202202255436.html
2型糖尿病で血中グルカゴン濃度が高いという報告は以前からあったが、その高血糖に対する寄与度はインスリン分泌不全やインスリン抵抗性に比べて低いと考えられてきた。その理由の一つは、従来の測定系で検出された2型糖尿病患者の血中グルカゴン濃度は健常者に比べて軽度の上昇であり、さらに検体間のバリエーションが大きく、統計学的有意差がつきにくかったからである。このような背景から、2型糖尿病ではまずβ細胞機能障害が先行し、その後2次的にα細胞機能障害が起きると考えられてきた。実際、β細胞から分泌されるインスリン、GABA、亜鉛などが隣接するα細胞のグルカゴン分泌を抑制するという研究成果が多く存在するし、α細胞特異的インスリン受容体欠損マウスのグルカゴン分泌は障害されていることも報告されている。ところが最近、筆者らはα細胞にはグルコース輸送体であるGLUT1とグルコース/Na+の共輸送体であるSGLT1の両方が発現していることを見出しており、高血糖や糖尿病状態では前者が減少し、後者が増加することでグルカゴン分泌が亢進するというメカニズムを提唱した。さらに最近、糖尿病モデルマウスのα細胞では分岐鎖アミノ酸(BCAA)の代謝酵素の発現量が変化しており、BCAA代謝異常が生じる結果、グルカゴンが過剰に分泌されるというメカニズムも報告した。従って、2型糖尿病ではβ細胞障害と並行してα細胞にも何らかの代謝異常が生じている可能性が高い。
インスリンは、膵臓のβ細胞から分泌され、血液中の糖を体内に取り込むことで血糖値を低下させるホルモンだ。一方のグルカゴンは、同じ膵臓のα細胞から分泌され、肝臓での糖産生を増やして血糖値を上昇させる働きがあり、血糖値が低下すると分泌される。インスリンとグルカゴンは、それぞれバランスを取りながら血糖値を一定に保っていることから、これまで「拮抗ホルモン」と捉えられてきた。
ところが、2010年と2011年に相次いで、グルカゴンに関する重大な発見があった。遺伝子改変動物を用いた基礎研究でのことである。
グルカゴンの作用が阻害されたα細胞欠損マウスやグルカゴン受容体欠損マウスは、薬剤投与によりβ細胞を破壊しインスリン分泌を阻害しても、正常な血糖値を維持することが明らかになった。さらに2012年には、血糖値の上昇には、インスリンの欠乏よりも、グルカゴンの上昇の方が重要であるとする「グルカゴン中心説」が発表されたのだ。
国内でも、2010年頃から、インスリン分泌促進だけでなく、グルカゴン分泌抑制作用を併せ持つ薬剤、インクレチン製剤が発売されたことで、あらためてグルカゴンに注目が集まるようになった。
